

本附属学校園では,本校および宇都宮大学,そして附属小学校と連携し,「主体的な問題解決を通して妥当な考えを創り出す児童・生徒を育む理科授業」をテーマと設定し,研究に取り組んでいる。具体的には児童・生徒らの主体的な問題解決活動において,既習の知識を活用し,思考や表現を他者と関わりながら共有したり,観察・実験の結果から結論を導き出す過程を最後までやり遂げたりすることを支援する。これらを通して,児童・生徒ら自身で「妥当な考え」,すなわちその学びの時点でもっとも科学的に確からしい考えを創り出す力を育成することが,本附属学校園理科の研究の目的である。
今回は,実践として第3学年に行った「水の電気分解のしくみについて深く考える」について紹介する。
第3学年の「化学変化とイオン」の単元では,目に見えないイオンや電子の存在,そしてそれによって起こる化学変化を,実験などを通じて理解していく必要がある。しかし,実験の結果や化学反応式を記憶することに難を感じ,この分野に対し苦手意識をもつ生徒も少なくない。実験の結果や化学反応式を単に記憶しようとするのではなく,実験の結果をもとに演繹的に考え,化学反応式を導き出す力を育成する必要がある。そのためには,起こった現象からその起因を個人や班で演繹的に考え,自分が学習している時点における「妥当な考え」を創り出す活動や,現象を説明し化学反応式を導き出す活動を生徒の学習レベルに応じて意図的に授業に取り入れる必要があると考える。
本時では,中学2年生で学習した水の電気分解について,3年生で得た既習概念を活用し改めて深く考察する活動を取り入れた。
実践の展開を表1に示す。本実践では,学習課題を2つ設けた。1つは「陰極付近が赤く変化した理由を説明する。」,もう1つが「陽極側で起きている反応を説明する。」である。ここでは,この課題を設定した理由や授業の場面ごとに授業者が配慮したことなどについて述べていくことにする。
表1 実践の展開
| 学習活動 | 指導上の留意点 |
|---|---|
課題1:陰極付近が赤く変化した理由を説明する。 |
|
|
※まず個人で考える時間を設ける。
|
課題2:陽極側で起きている反応を説明する。
|
※既習概念や原子モデルを使い,わかりやすく説明ができるよう,アドバイスを行う。
|
|
|
|
|
通常水の電気分解の実験は,水酸化ナトリウムを少量水に溶解させ,通電性を高めて行われる。しかし今回は,液性を中性に留めるために水酸化ナトリウムの代わりに硫酸ナトリウムを溶かした水溶液を用いた。これにより,使用する水溶液に指示薬を垂らし通電した際,両極の液性変化が視覚的に理解できることをねらった。
まず,2年生で行った実験の際には,水に少量の水酸化ナトリウムを溶解させたことから,その条件で仮に電気分解で使用した水溶液にフェノールフタレイン溶液を滴下した場合は何色を呈するか生徒に問いかけた。また,実際に水溶液が赤色を呈する事を演示で確認する。そして,今回の実験では,水酸化ナトリウム水溶液を使用せず,硫酸ナトリウム水溶液を使用することや硫酸ナトリウムの化学式(Na2SO4)を説明する。また,今回の反応において,硫酸ナトリウムは通電性を高める存在であり,直接的に水の電気分解には作用しないことも伝えた。
導入場面の後,この水溶液にフェノールフタレイン溶液を数滴垂らし電気分解を行った際,両極付近でどのような色の変化が起こるかを予想させた。事前の授業において,生徒は水が微少ながら水素イオンと水酸化物イオンに電離していることや,中和反応によって水が生成されることを学習している。そのためか,図1のようにほとんどの生徒は,+のイオンである水素イオンが陰極へ,-のイオンである水酸化物イオンが陽極側へ引きつけられ「陽極側が水酸化物イオンの影響を受け赤く染色される」と予想した。


図1 生徒の予想

図2 反応のようす

図2 反応のようす
しかし,実際に生徒実験を行うと,図2のように「陰極側が赤く染まる」という結果が出る。この実験結果に疑問の声を上げながらも,なぜこのような現象が起こったのかをすぐに考え始める生徒が多く見られた。自分の予想と逆の結果が出ることは,生徒の探究する意欲を高めることや,現時点で自分が有している知識を活用して「妥当な考え」を導き出そうとする態度を育成することに大きく寄与することが考えられる。

図3「分かっていること」

図3「分かっていること」
本実践では,まず個人でじっくりと課題に向き合う時間を設けた。そこでは,なぜ陰極付近が赤く変化したのかを,じっくりと粘り強く考える生徒の姿が見られた。水酸化ナトリウムの代わりに溶解させた硫酸ナトリウムが関係しているのではないか,と授業者にその化学式や電離式を質問したり,論理を進めるために現時点で「分かっていること」を書き出したりしていた。図3は,生徒のワークシートに書かれていた「分かっていること」の例である。2年生で学習した水の電気分解の化学反応式や電離のようす,フェノールフタレイン溶液の性質を書く生徒など,現在自分が分かっていることを書き,様々な角度からこの課題を説明するための「妥当な考え」を導き出そうとする生徒のようすがあった。
本実践を含め,本校の理科授業では,以下の2点を重要な手立てとして考え取り組んでいる。
・個人でじっくりと課題に向き合う時間をとる
班で協力し課題を解決する活動は,理科授業の中で大きな効果を持つ活動である。またそこから得られる生徒の資質・能力は,当然今後も理科教育で養うべき力のひとつであるといえる。ただし,やみくもに班で活動をするのでは,その効果が薄れてしまうことが考えられる。まずは,個人で粘り強く課題に向き合い,自分の考えをしっかりともち,その上で班での活動に臨むことが重要である。
・「分かっていること」と「自信のないところ」を明記する
生徒が,自分の有する概念を総合的に活用し課題を解決するためには,現時点で「分かっていること」や逆に「自信のないところ」を明確にしながら,自分の論を進める必要がある。それは「妥当な考え」を導き出すために,自分が現在どの地点に立っているのかを分かること,すなわちメタ認知を行いながら,課題の解決に臨むことが重要であると言い換えることができる。
本実践では,特に現時点で「分かっていること」を図3のようにワークシートに明記し,自分の論を整理するよう生徒へ働きかけた。また,必要に応じてクラス全体で「分かっていること」の共有を行った。先述のように,生徒は,理論の中のどこに今自分がいるのかを明確にすることで,演繹的に考えを絞ることができ,その結果1つの妥当性のある考えを導き出すことができる。

図4 原子モデル

図4 原子モデル
課題2では,授業者が作成した原子モデル(図4)を各班に配り,陽極側で起きていると考えられる化学反応を班で考え説明することを生徒に求めた。今回作成した原子モデルは,水素イオン(Ⓗ+)と酸素原子(Ⓞ),水素原子(Ⓗ),電子(
 )をそれぞれ4つずつ(水分子4つ分)である。それらを結びつけたり離したりしながら,陽極側での反応(4OH- → 2H2O + O2 + 4e)を導き出し説明することが求められる。
)をそれぞれ4つずつ(水分子4つ分)である。それらを結びつけたり離したりしながら,陽極側での反応(4OH- → 2H2O + O2 + 4e)を導き出し説明することが求められる。
生徒に対しては,必要な情報があれば授業者に随時質問するように指示し,各班の進捗状況を見ながら,解決に必要な情報を徐々に全体へ共有するように心がけた。中学3年生が目に見えないイオンや電子を捉え,上記の化学反応式を導き出すことは非常に難しいことである。しかし,今回の実践では,現時点で「分かっていること」を整理したりクラスで共有したりすることで,多くの班が演繹的に「妥当な考え」を導き出し,陽極側での化学反応を説明することができていた。
表2 課題解決に必要な情報
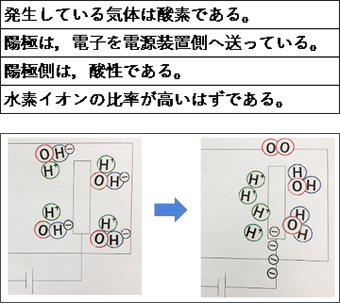
図5 陽極での反応
表2 課題解決に必要な情報

図5 陽極での反応
では,陽極側で起こっている反応を説明するためには,どのような情報が最低限必要とされるのだろうか。その代表例を表2に示す。生徒は,これらの情報を総合的に用い,現在の学びにおける「妥当な考え」を創り出していたということが言える。ただ見当もつけずにモデルを動かしながら,4つのOH-から酸素分子2つと水分子2つ,電子4つを作り出すようなことは,運良くできるものではない(図5)。この課題を解決するためには,課題1から見えてきた陰極でのようすや必要とされる情報,これまで学習してきた概念を総合的に活用し,演繹的に論を進めることが必要不可欠なのである。
図6は,課題2に関する生徒のワークシートである。よく注視してみると,簡単に自分の考えを導き出せるわけではなく,理論的には間違っている部分も見られる。しかし,友人の意見や発表を参考に最終的には,「妥当な考え」を導き出すことができていることが分かる。
また,課題2における班での話し合いの中に,「水酸化物イオン(OH-)を酸素原子(Ⓞ),水素原子(Ⓗ),電子(
 )に分解することができるのか」という内容のやりとりを行っている場面が見られた。私たち授業者にとっては,電荷数さえ間違わなければ原子レベルまで分解することは当然可能であることは分かっている。しかし,生徒にとって水酸化物イオン(OH-)は,もうこれ以上分解できないひとつの形であるという固定概念が存在するのではないかと考えられる。水素イオンや酸化物イオンのような1種類の原子における電子の貸し借りについては学習している。水酸化物イオンやアンモニウムイオンのような2種類以上の原子が結びついたイオンを原子と電子に分解するというアイデアは,なかなか難しいということが実感された。
)に分解することができるのか」という内容のやりとりを行っている場面が見られた。私たち授業者にとっては,電荷数さえ間違わなければ原子レベルまで分解することは当然可能であることは分かっている。しかし,生徒にとって水酸化物イオン(OH-)は,もうこれ以上分解できないひとつの形であるという固定概念が存在するのではないかと考えられる。水素イオンや酸化物イオンのような1種類の原子における電子の貸し借りについては学習している。水酸化物イオンやアンモニウムイオンのような2種類以上の原子が結びついたイオンを原子と電子に分解するというアイデアは,なかなか難しいということが実感された。

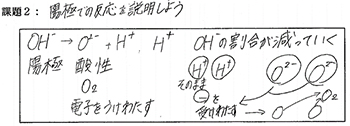
図6 生徒のワークシート
本実践では,上記のように自分の予想と反する現象について,粘り強く考え「妥当な考え」を創り出す生徒の姿が見られた。
今後の課題は,硫酸ナトリウムより通電性の高い中性の電解質を探すことである。本実践に用いた硫酸ナトリウムは,12V程度の電圧を加え実験を行う必要があった。また,フェノールフタレイン溶液による陰極付近での反応は観察できたが,あまり酸素と水素の気体が発生しているようすを観察することができなかった。中性であり,かつより通電性が高い物質を用いることで,より反応が分かりやすく観察でき,生徒の思考も深まることが期待できる。